增值电信业务经营许可证是由国家工信部或各省通信管理局办法的合法经营特定电信业务的法定资质证书。
企业想要合法开展互联网信息服务、在线数据处理与交易处理(如电商平台)等业务,都必须先取得相应的许可证。无证经营将面临没收违法所得、处违法所得3-5倍💰罚款,或无违法所得时处以10万至100万元罚款,情节严重的还可能被责令关闭网站。

更多证书办理详情可直接与我们方圆盛世网站在线客服联系,或电话咨询官方热线:400-090-3278
在申请前,首先要判断自己的业务属于哪一类。根据《电信业务分类目录》,增值电信业务分为两类:
第一类增值电信业务(以设施资源为主)
包括IDC许可证(互联网数据中心)、CDN许可证(内容分发网络)、ISP许可证(互联网接入服务)、VPN许可证(互联网虚拟专用网)等。
第二类增值电信业务(以公共应用平台为主)
与大多数互联网企业关系更密切,也是申请量最大的类别,主要包括:
● ICP许可证(B25类):通过互联网提供经营性信息服务。涉及付费会员、付费阅读、广告投放、信息社区、即时交互等业务的网站/App均需办理。→办理最多
● EDI许可证(B21类):在线数据处理与交易处理业务。存在第三方商家入驻并涉及资金交易的电商平台(如淘宝、美团)必须持有。
● 呼叫中心许可证(B24类):以95/96号码提供呼叫服务。
● SP许可证(B25类非互联网):通过短信、彩信等移动网提供信息服务。
● 多方通信许可证(B22类):提供多方语音通话或视频会议服务。
● 存储转发类业务(B23类):如语音信箱、电子邮件等。
注意⚠️:如果仅通过自营网站/APP以自营方式直接销售商品、自行发布信息(非为他人提供平台),或依托微信/支付宝的小程序/公众号经营且无独立平台,无需❌申请增值电信业务经营许可证。
⭐️ ICP备案与ICP许可证
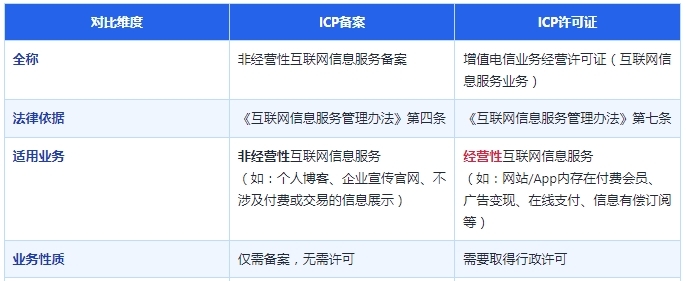
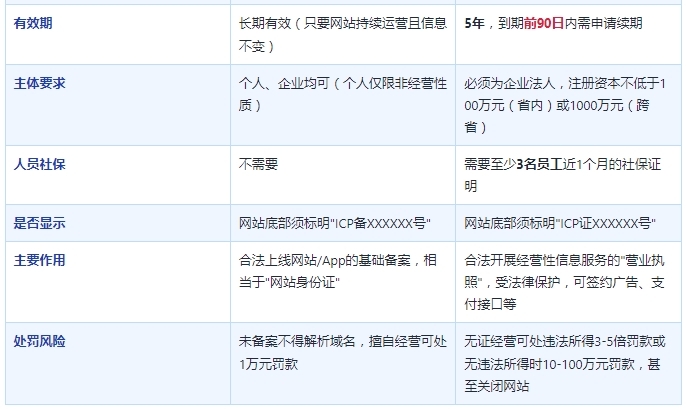
很多人搞不清ICP备案和ICP许可证,什么情况ICP备案就行了,什么情况必须办理ICP许可证,简单一句话概括下:
所有上线服务的网站/APP/小程序等均需要做ICP备案,如果这些网站/APP/小程序还涉及收费性质,如会员费、订阅费、道具费、广告费等,则需要进一步办理ICP许可证。
申请条件
● 申请主体须为企业,个体工商户办不了;
● 经营范围含"第一类增值电信业务"或"第二类增值电信业务";
● ICP和EDI注册资金不低于100万,其他不低于1000万
● 已备案域名登记证书;
● 提供三名人员近一个月社保记录;
● 有符合条件的网站、技术方案、经营场地;
● 法人或主要负责人近三年无违法违规或电信业务不良记录等。










